[비즈월드] “세계 2위의 바이오 의약품 생산능력, 한미 백신 파트너십 등에 기반해 인류 공동의 감염병 위기 극복에 앞장설 것"이라며 "내년 상반기까지 국산 1호 백신을 상용화하는데 정부가 기업과 함께 하겠다.”
문재인 대통령이 15일 서울 중구 문화역서울284(구 서울역사)에서 열린 제76주년 광복절 경축식 경축사에서 "백신 접종이 목표에 다가가고 있다. 델타 변이 확산으로 인한 4차 유행도 반드시 이겨낼 것"이라며 덧붙인 내용이다.
문 대통령은 "대한민국은 역사의 중요한 분기점에서 선도국가로 나아갈 기회를 맞고 있다. 코로나 위기 극복 및 코로나 이후 세계 경제 재건, 평화질서에 적극 이바지할 것"이라면서 ▲백신 허브 국가 도약 ▲글로벌 공급망에서 한국의 역할 제고 ▲선도적인 저탄소 경제 전환 추진 등 3대 목표도 제시했다.
정부의 공언을 뒷받침 해주는 바로미터가 되는 것이 관련 특허의 출원과 등록 현황이다.
코로나19의 게임 체인저로 떠오를 치료제 개발이 주목받고 있다. 글로벌 제약사들도 경구용 치료제 개발을 위해 임상시험에 돌입하는 등 경쟁도 치열해지고 있다.
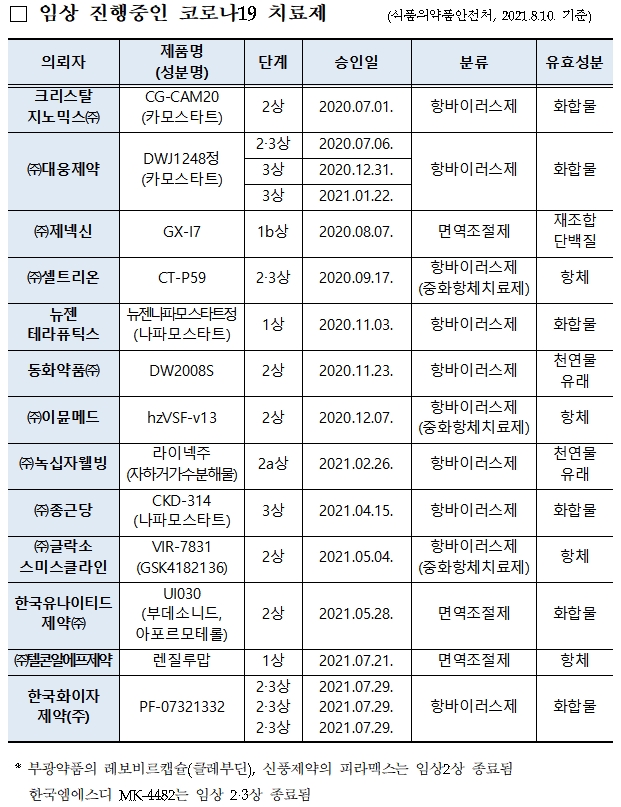
유례없는 사태를 겪고 있는 전 세계 각국은 사활을 걸고 코로나19 치료제 개발에 심혈을 기울이고 있다. 우리나라의 경우 지난 2월 국내 최초의 코로나19 치료제로 렉키로나주가 정맥주사제로서 조건부 허가를 받은 이후, 제약사 및 연구소들이 국내 치료제 개발을 위해 속도를 내며 관련 특허 출원도 이어지고 있다.
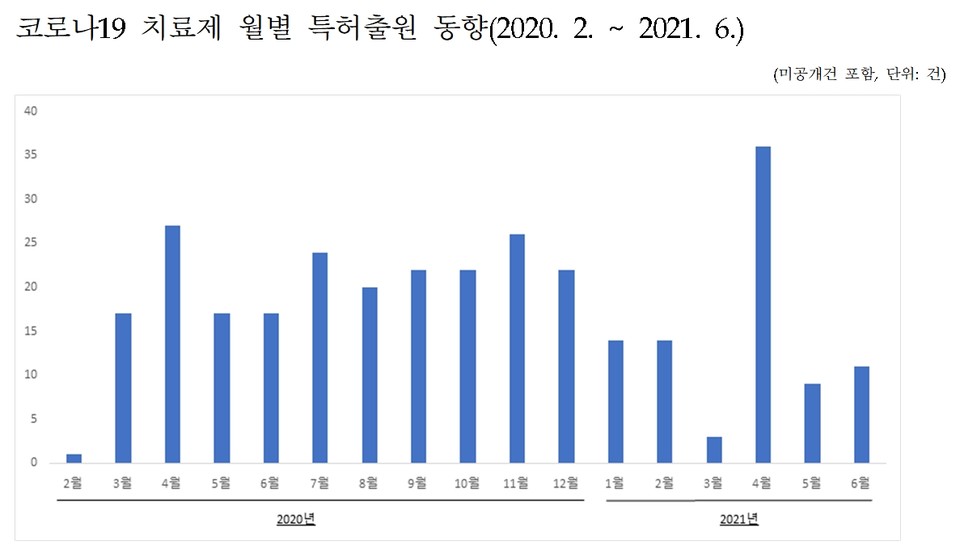
16일 특허청(청장 김용래)에 따르면 코로나19 치료제 관련 특허출원은 코로나19 발병 초기인 2020년 2월부터 꾸준히 출원돼 지난 6월까지 총 302건이 출원됐다.
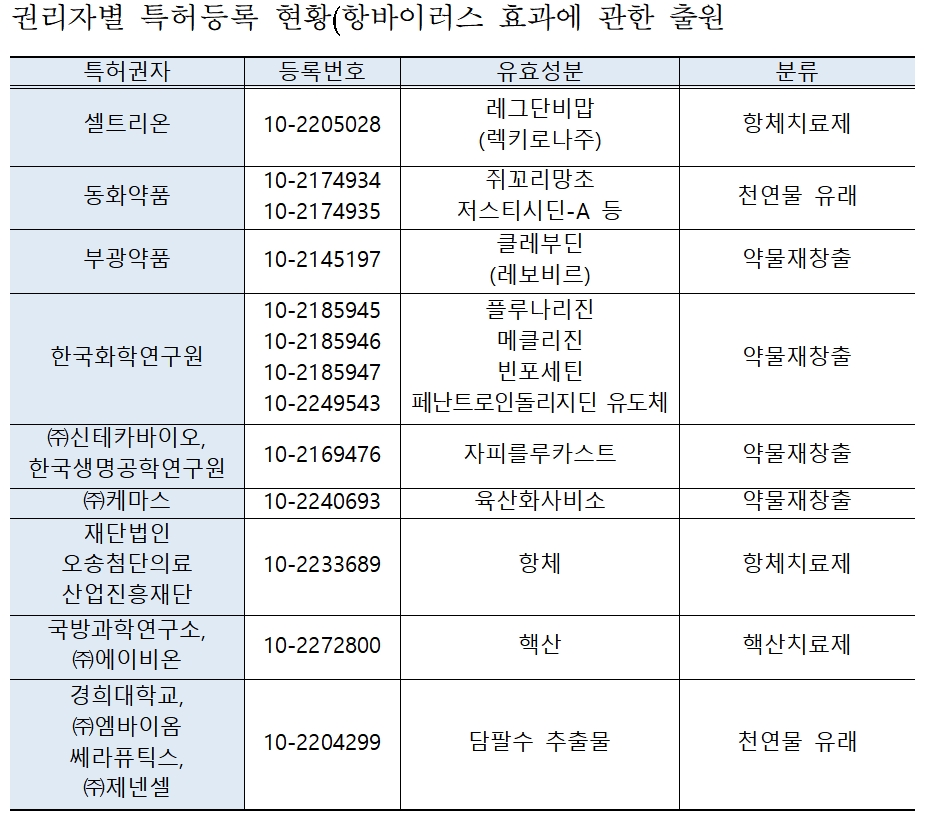
현재 코로나19에 대한 항바이러스 효과로 특허 등록된 출원은 총 13건이었다. 이 중 코로나19 치료제로 허가를 받은 특허는 셀트리온의 ‘렉키로나주(레그단비맙, 항체치료제 특허 등록번호 제102205028호)’가 있으며 임상 진행 중인 특허는 동화약품의 ‘DW2008S(쥐꼬리망초 유래 신약, 등록번호 제102174934호, 등록번호 제102174935호)’ 등 2건, 임상 종료된 특허는 부광약품의 ‘레보비르(클레부딘, 약물재창출, 등록번호 제102145197호)’ 1건 등이 포함됐다.
이밖에 한국화학연구원의 ‘플루나리진’, ‘메클리진’, ‘빈포세틴’, ‘페난트로인돌리지딘 유도체’(이상 각각 등록번호 제102185945호, 제102185946호, 제102185947호, 제102249543호)와 ㈜신테카바이오-한국생명공학연구원의 ‘자피를루카스트(등록번호 제102169476호)’, ㈜케마스의 ‘육산화사비소(등록번호 제102240693호)’, 재단법인 오송첨단의료 산업진흥재단의 ‘항체 등록번호 제102233689호)’, 국방과학연구소-㈜에이비온의 ‘핵산(등록번호 제102272800호)’, 경희대학교-㈜엠바이옴 쎄라퓨틱스-㈜제넨셀의 ‘담팔수 추출물(등록번호 제102204299호)’ 등이 대표적이다.
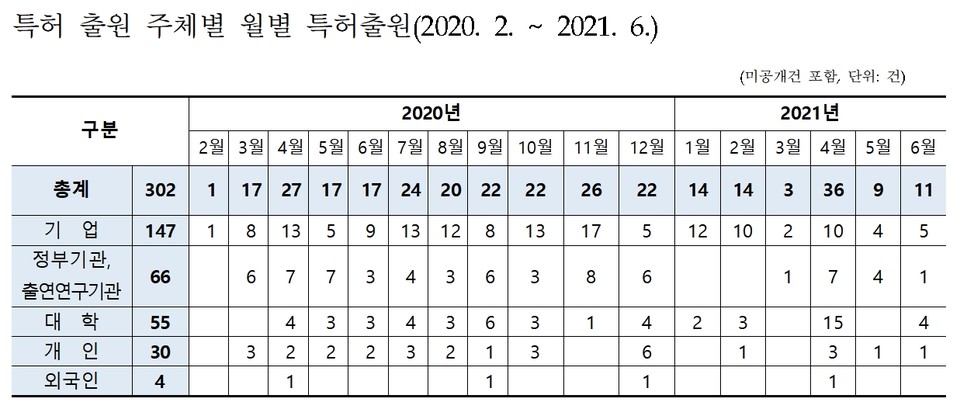
코로나19 치료제 특허를 출원인별로 보면 국내 제약사 등 기업이 147건, 정부기관 및 출연연구소가 66건, 대학이 55건, 개인이 30건, 외국인이 4건이었다.
국내기업의 특허출원이 전체 출원 중 48.7%로 많은 비중을 차지했다. 이어 정부기관 및 연구소 21%, 대학 18% 등 순이었다.
외국인 특허는 국제출원 후 31개월 내 국내 출원하면 되기 때문에 대부분이 아직 국내 특허 단계에는 진입하지 않은 상황으로 특허청은 분석하고 있다.
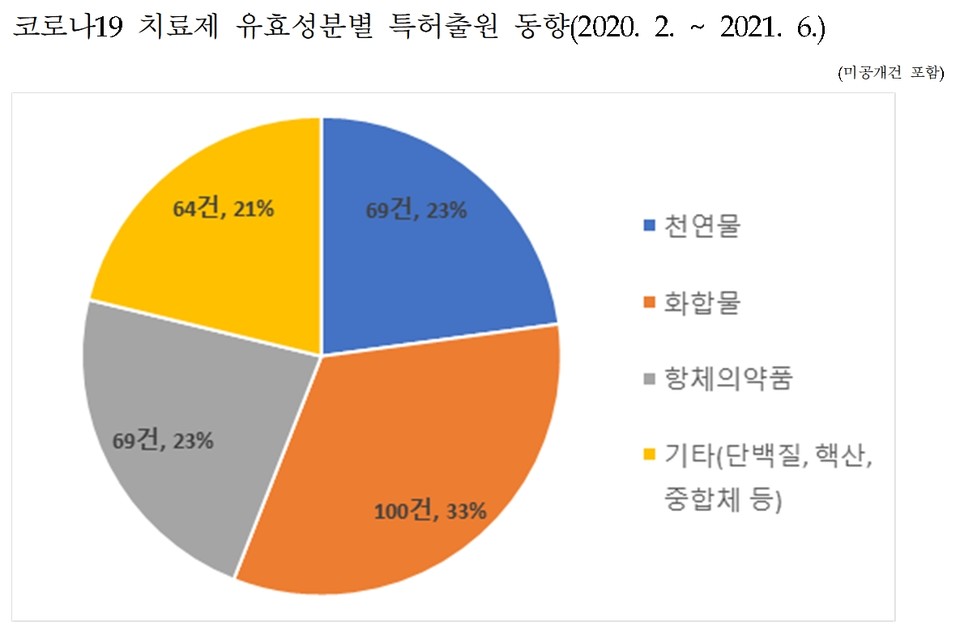
국내 출원된 코로나19 치료제는 유효성분에 따라 화합물, 항체의약품, 천연물 등으로 나뉜다.각각 100건, 69건, 69건의 특허가 출원됐다.
이 가운데 제약사들은 신약 개발과 함께 단기간 내 치료제를 개발하기 위해 기존 의약품을 활용한 ‘약물 재창출 방식’ 등 다양한 시도를 하는 것으로 분석된다.
여기서 ‘약물 재창출 방식’이란 이미 치료제로 사용되고 있는 약물을 다른 질병의 치료제로 가능성을 탐구하는 전략으로 신약 개발에 투자되는 비용과 기간을 크게 줄일 수 있는 점이 장점으로 만히 활용되고 있다.
특허청은 코로나19 치료제 특허는 국가연구개발사업 기반으로 정부기관 및 연구소, 대학, 기업의 특허출원이 이어지는 것으로 분석했다.
국가 연구개발사업을 기반으로 출원된 건이 전체(302건)의 25.8%(78건)로 일반적으로 국가 연구개발사업에 따른 특허 출원은 전체 출원의 15% 미만에 비해 많았다.
앞서 정부는 지난해 4월부터 ‘코로나19 치료제·백신 개발 범정부지원위원회’를 가동해 국산 코로나19 치료제의 개발을 지원하고 있다. 이에 따라 관련 분야 특허 출원이 더 활발할 것으로 기대되고 있다.
그렇다면 글로벌 제약사들의 코로나19 치료제 개발은 어떤 상황일까?
특허청이 분석한 결과 글로벌 제약사들도 역시 코로나19 치료제 개발에 한창이다. 미국 FDA지난 8월 3일 기준으로 일라이 릴리, 리제네론, 제넨텍, GSK의 정맥주사제와 길리아드의 렘데시비르 등 총 11개 치료제에 대해 긴급사용승인을 했고 그중 렘데시비르만 정식으로 허가했다
미국 머크(MSD)사는 경구용 치료제 몰누피라비르 개발에 집중하고 있고, 임상시험 결과에 따라 연내 FDA 긴급사용승인도 이뤄질 것으로 예상되고 있다. 타미플루를 개발했던 로슈도 경구용 코로나 치료제로 임상을 진행하고 있으며 화이자도 경구용 치료제 임상을 진행 중이다.
곽희찬 특허청 약품화학심사과 심사관은 “과거 신종플루의 사례에서 알 수 있듯이 코로나19를 종식시키는 데는 간편하게 복용할 수 있는 치료제의 개발이 절실하다”면서 “국내외 제약사들도 신물질개발, 항체치료제, 약물재창출 방식 등 다양한 방법으로 코로나19 치료제 개발을 위해 노력하고 있다”라고 설명했다.
이어 “특허발명을 의약품으로 사용하려면, 추가적인 기술개발이 필요할 수 있고 임상시험 결과에 기초한 안전성 및 유효성 심사를 거쳐 식약처의 허가를 받아야 한다”며 “의약품은 특허를 등록받았다고 해서 바로 사용할 수 있는 것은 아니다. 꼼꼼한 사후 절차가 있음을 유의해야 한다”라고 강조했다.
관련기사
- [페이턴트] “세계 車 생산업체의 화두인 ‘전기차 개발’”…배터리 관련과 함께 ‘핫스탬핑’ 특허 선점 경쟁 치열
- [페이턴트] 소비자에게 익숙한 장수상표를 활용 이색 협업상품 출시 붐…비즈월드 단독보도 ‘국내 최초 출원 상표’는 선미제과의 '해태'
- [페이턴트] "코로나19 영향에 늘어난 ‘홈트족’"…덩달아 비대면·스마트 기술 적용한 실내 운동기구 특허출원 급증
- [페이턴트] “코로나 영향에 등락 엇갈린 디자인 특허 출원”…생활·위생용품 vs 뷰티·쥬얼리
- [페이턴트] 급증한 온라인쇼핑…덩달아 물류운송 관련 특허 기술도 AI·IOT 결합으로 진화·급증
- [페이턴트] “코로나19 뚫은 한국 발명가들의 열정”…올해 상반기 국제출원, 특허·상표·디자인 4·10·1위 랭크
- [페이턴트] “긴 터널 벗어나려는 국내 코로나 사태”…올해 8월 말까지 코로나 관련 지정상품 출원 전년 比 107.7% ↑
- [페이턴트] “저탄소경제 시대 신재생에너지 대표 주자 ‘태양전지’를 더 효율적으로”…'페로브스카이트 태양전지' 관련 특허출원 급증
- [페이턴트] “2022년, 특허출원 대세는 ‘메타버스’”…IP5, 최근 10년간 실감형 콘텐츠 관련 특허출원 연평균 19%↑
- [페이턴트] “코로나에도 인기 치솟는 ‘골프’”…덩달아 골프 관련 디자인 출원 급증
- [페이턴트] 2022년 신기술의 화두 ‘메타버스’…‘K-POP’ 기획사들도 메타버스 대세 흐름에 승차

